- 20/09/2020
- 34
- 13
- 32
Salve pessoal, bom dia!!
Preparei 6 potes de cultura líquida, todos com self-injection ports feitos com silicone que suporta altas temperaturas e um pequeno buraco tampado com micropore para a troca gasosa.
Procedimentos:
1- Deixei água mineral fervendo, conforme sugerido no tutorial (do @tupy) que li sobre cultura líquida, para depois adicionar dextrose anidra comprada em loja especializada de produtos laboratoriais.
2- Enquanto fervia a água mineral, eu limpei os potes com alcool 70%, borrifando dentro de todos eles e depois passando um papel toalha para retirar o excesso. (Eu não coloquei-os em água fervente conforme foi ensinado no tutorial porque já imaginei que eles seriam esterilizados quando fosse pra panela de pressão)
3- Assim que a água foi fervida, adicionei a dextrose em um bécker e depois joguei a água fervida dentro dele e misturei. Eu usei a proporção indicada no tutorial que foi de 2g de dextrose para 250ml de água.
4- Logo após isto eu distribui a solução nos seis potes, coloquei papel laminado em cima de todos, e coloquei eles para serem esterilizados na panela de pressão durante 20 minutos contados a partir do momento em que a panela a pega pressão.
5- Esperei a panela esfriar naturalmente e perder toda a pressão para depois inocular os potes com seringa de esporos hidratada (já utilizada em potes de milho e que estão colonizando de forma saudável, ou seja, parece uma seringa saudável).
6- Dentro de uma SAB preparada previamente com alcool 70% e lisoform, eu limpei os potes com alcool 70 antes de colocar na SAB e fiz a inoculação a partir da self-injection port de silicone como foi dito anteriormente. Após a inoculação foram direto para incubadora a uma temperatura de 27-28 graus celsius.
Observações:
Dentro de uma semana, se não tiver enganado, não observei nenhum crescimento de micélio nas soluções de dextrose. E só no 12º dia que somente UM pote começou a aparecer o micélio, motivo de comemoração rsrs. No entanto, os demais basicamente sem nenhum rastro de micélio. O que eu percebi é que em alguns potes, durante a inoculação com a seringa multi esporos, pequenos fragmentos de silicone caíram dentro da solução. O que eu imagino é que eles devem ter ressecado na panela de pressão e ai assim que eu injetei a agulha, alguns pedaços minúsculos acabaram se despregando da tampa, o que é estranho porque o silicone deve suportar tranquilamente a temperatura dentro da panela de pressão (muitas pessoas usam o silicone e tem sucesso pelo que vejo).
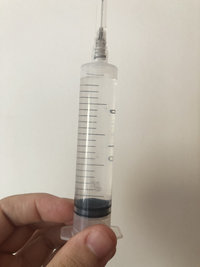
Hoje faz 19 dias que, esse único pote que teve o micélio desenvolvido, está na incubadora. Eu notei dias atrás a formação de pequenos pontos pretos no meio da solução. Estou anexando as fotos para que possam ver como está e me darem alguma sugestão do que possa ser esses pontos. Engraçado é que quando fui fazer uma CL (minha primeira usando seringa com soro glicosado), ela desenvolveu uma pequena (muito pequena) quantidade de micélio com esse pontinho preto. E quero deixar claro que não sei se é realmente micélio ou algum contaminante.
Quem puder dar um help, valeeeu!
Preparei 6 potes de cultura líquida, todos com self-injection ports feitos com silicone que suporta altas temperaturas e um pequeno buraco tampado com micropore para a troca gasosa.
Procedimentos:
1- Deixei água mineral fervendo, conforme sugerido no tutorial (do @tupy) que li sobre cultura líquida, para depois adicionar dextrose anidra comprada em loja especializada de produtos laboratoriais.
2- Enquanto fervia a água mineral, eu limpei os potes com alcool 70%, borrifando dentro de todos eles e depois passando um papel toalha para retirar o excesso. (Eu não coloquei-os em água fervente conforme foi ensinado no tutorial porque já imaginei que eles seriam esterilizados quando fosse pra panela de pressão)
3- Assim que a água foi fervida, adicionei a dextrose em um bécker e depois joguei a água fervida dentro dele e misturei. Eu usei a proporção indicada no tutorial que foi de 2g de dextrose para 250ml de água.
4- Logo após isto eu distribui a solução nos seis potes, coloquei papel laminado em cima de todos, e coloquei eles para serem esterilizados na panela de pressão durante 20 minutos contados a partir do momento em que a panela a pega pressão.
5- Esperei a panela esfriar naturalmente e perder toda a pressão para depois inocular os potes com seringa de esporos hidratada (já utilizada em potes de milho e que estão colonizando de forma saudável, ou seja, parece uma seringa saudável).
6- Dentro de uma SAB preparada previamente com alcool 70% e lisoform, eu limpei os potes com alcool 70 antes de colocar na SAB e fiz a inoculação a partir da self-injection port de silicone como foi dito anteriormente. Após a inoculação foram direto para incubadora a uma temperatura de 27-28 graus celsius.
Observações:
Dentro de uma semana, se não tiver enganado, não observei nenhum crescimento de micélio nas soluções de dextrose. E só no 12º dia que somente UM pote começou a aparecer o micélio, motivo de comemoração rsrs. No entanto, os demais basicamente sem nenhum rastro de micélio. O que eu percebi é que em alguns potes, durante a inoculação com a seringa multi esporos, pequenos fragmentos de silicone caíram dentro da solução. O que eu imagino é que eles devem ter ressecado na panela de pressão e ai assim que eu injetei a agulha, alguns pedaços minúsculos acabaram se despregando da tampa, o que é estranho porque o silicone deve suportar tranquilamente a temperatura dentro da panela de pressão (muitas pessoas usam o silicone e tem sucesso pelo que vejo).
Hoje faz 19 dias que, esse único pote que teve o micélio desenvolvido, está na incubadora. Eu notei dias atrás a formação de pequenos pontos pretos no meio da solução. Estou anexando as fotos para que possam ver como está e me darem alguma sugestão do que possa ser esses pontos. Engraçado é que quando fui fazer uma CL (minha primeira usando seringa com soro glicosado), ela desenvolveu uma pequena (muito pequena) quantidade de micélio com esse pontinho preto. E quero deixar claro que não sei se é realmente micélio ou algum contaminante.
Quem puder dar um help, valeeeu!